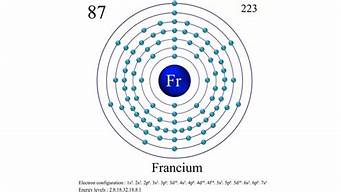
1.原子的组成
1.原子的体积非常小。将原子与乒乓球进行比较,就像将乒乓球与地球进行比较一样。当人们研究微小的原子结构时,原子如何结合形成分子的奥秘逐渐被揭开。 2.原子的结构。
原子由位于原子中心的带正电的原子核和位于原子核外的带负电的电子组成。原子核由质子和中子组成。原子核位于原子的中心,体积很小。原子中有一个很大的空间,电子在这个空间中高速运动。
[注]
(1)并非所有原子的原子核中都有中子,例如氢原子中只有一个质子和一个核外电子,但没有中子;
(2) 核电荷数=质子数=核外电子数;
(3) 一个原子的质子数(或核电荷数)原子决定了原子的类型,因此不同类型的原子在原子核中具有不同数量的质子。
(4)原子核中的质子数和中子数不一定相等,例如钠原子核中有11个质子和12个中子。
二、电子在原子核外的排列
与原子相比,原子核的体积更小。如果把原子比作一个体育场,那么原子核只相当于体育场中的一只蚂蚁。所以原子核外有很多空间。电子在这个空间中高速运动。
科学研究表明,在含有多个电子的原子中,原子核外的电子具有不同的运动状态。最近的电子层是该层,其次是第二层,依此类推为第三、第四、第五、第六和第七层。外层也称为外层。电子在原子核外的这种分层运动也称为分层排列。已知原子核外的电子壳层数少则多则多则多于七层,而外层电子层数不超过8个(外层电子层数不超过不超过2)
利用原子结构示意图可以简洁方便地表达核外电子的层状排列。
[核外电子排列规律]
(1)层内最多容纳2个电子。
(2) 第二层最多只能容纳8个电子。
(3)最外层电子数不超过8个。 (如果壳层电子数是最外层的,不超过2个)
二、相对原子质量
1。原子的体积非常小。将原子与乒乓球进行比较,就像将乒乓球与地球进行比较一样。当人们研究微小的原子结构时,原子如何结合形成分子的奥秘逐渐被揭开。
以上是以碳原子(碳12,其原子核中有6个质子和6个中子)质量的1/12为标准,与其他原子的质量比较得到的数值值是原子的相对原子质量。
2.原子的结构。
某原子的相对原子质量(Ar)=
[注]
(1)相对原子质量是一个比值,没有单位;
strong>
p>
(2) 相对原子质量越大,原子的实际质量就越大。
(3) 近似的相对原子质量=质子数+中子数
3.原子质量与相对原子质量的区别
原子质量
相对原子质量
推导与性质
测定,
比较,相对
< p>取值和单位
很小,有单位
大于等于“1”,单位为“1” ",一般不写
注:A、B两个原子的相对原子质量之比等于它们质量之比,成正比。
原子结构示意图(原子是由什么构成的)介绍到此结束。
文章来源于网络或者作者投稿,若有侵权请联系删除,作者:大象,如若转载,请注明出处:https://www.laoz.net/25756.html