教学目标:
知识与技能:
1.了解工业上如何将铁从铁矿石中转化 还原的方法。 2.掌握实验室一氧化碳与氧化铁反应的实验过程及注意事项。
过程与方法:
通过对工业炼铁原理的讨论和研究,锻炼将知识应用到实际生活中的能力。
情感态度和价值观:
1.了解从铁矿石中回收铁的工业方法。 2.掌握实验室一氧化碳与氧化铁反应的实验过程及注意事项。
重点难点:
1.了解从铁矿石中还原铁的工业方法。 2.掌握实验室一氧化碳与氧化铁反应的实验过程和注意事项。 3.工业炼铁的化学原理。
教学过程
1.提出和讨论问题并创设情境:
1.日常生活中广泛使用的金属有哪些?
2.铁在自然界中以什么形式存在?
3.你知道我国什么时候发明了炼铁技术吗?
4.现代工业用什么技术把铁矿石变成铁?今天我们就来学习一下以铁矿石为原料冶炼铁的反应原理和过程。
其次,进行实验。
今天我们以主要成分为Fe₂O₃的赤铁矿为例,学习如何实现炼铁。 Fe2O3和Fe都含有Fe元素,不同的是Fe缺少O元素。将Fe₂O₃转化为Fe,可选择加入其他易氧物质与Fe₂O₃反应,通过吸氧还原Fe₂O₃。
从经济效益、反应是否充分、能源利用率等方面考虑,业界选择CO捕集Fe2O3中的O。为了更好地理解一氧化碳与氧化铁反应生成铁的过程,我们利用聚道VR/3D融合创新实验室进行实验,观察实验现象,分析实验过程。
组织学生进行正确的实验操作,观察并记录实验现象。
Video loading...
思考并讨论以下问题:
(1)为什么在一段时间内需要通过CO加热 Fe2O3 之前的实验?
(2)澄清石灰水的作用是什么?
(3)点燃喷嘴喷出的气体的目的是什么?
(4)先停止一氧化碳气体或关闭酒精喷灯,为什么?
(5) 如何验证实验中产生了铁?
分析完实验后,让学生试着写出一氧化碳与氧化铁的反应方程式。
注意:本实验需要强调实验的安全性。如果在涉及一氧化碳的实验中没有尾气处理装置,空气中的一氧化碳含量会越来越高,达到一定浓度就会引起中毒,甚至危及生命;如果一氧化碳气体与空气混合加热会发生爆炸,非常危险。
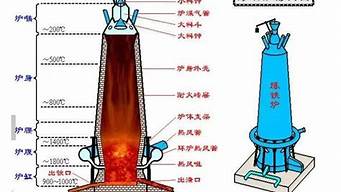
三、展示炼铁高炉模型,分析高炉炼铁过程。
概要:工业炼铁
设备:高炉
原料:铁矿石、焦炭、石灰石
尾气主要成分: CO和CO2(处理后排放)
展开:
展开:高炉炼铁为什么要用焦炭?
焦炭是将某种煤在焦化炉中保温,隔绝空气,强化热干馏而得到的一种硬质多孔固体。焦炭用于高炉炼铁。首先,它被用作热源。可乐在燃烧时会放出大量的热量。其次,生成的二氧化碳与焦炭在高温下反应生成还原剂一氧化碳。一氧化碳将铁矿石还原成铁。
焦炭质硬、多孔,在高炉中不易破碎,易让气体通过,热值比煤高,所以高炉用焦炭代替煤。
关于炼铁原理炼铁原理的化学方程式介绍到此结束。
文章来源于网络或者作者投稿,若有侵权请联系删除,作者:唐唐,如若转载,请注明出处:https://www.laoz.net/26670.html